Screening HCM
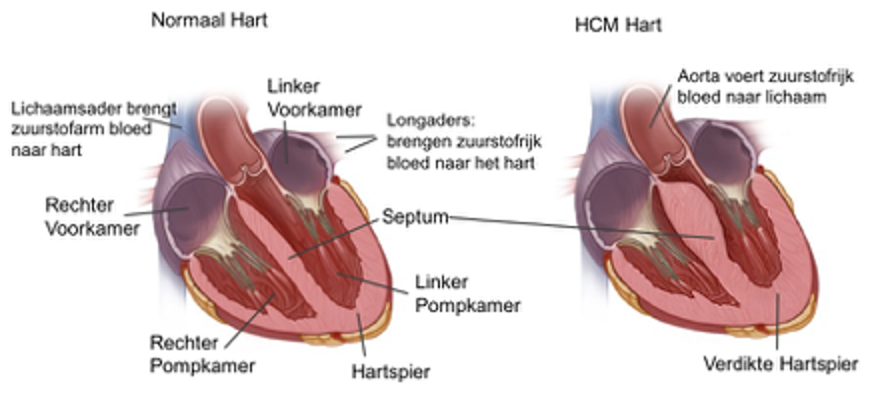
Hypertrofische CardioMyopathie, afgekort HCM, is een hartaandoening die wordt gekenmerkt door verdikking van de hartspierwand van de pompkamer, meestal de linker pompkamer. Omgezet in eenvoudige woorden: hypertrofisch = dikker worden, cardio = hart, myo = spier en pathie = ziekte.
Echografische screening van het hart wordt bij ons gedaan door Barbara Vandevelde. Barbara is Europees Specialist in Veterinaire Medische Beeldvorming (Dipl ECVDI) en mag officiële screenings uitvoeren voor PawPeds en andere instanties.
De katers worden best jaarlijks getest. Kattinnen worden jaarlijks of tweejaarlijks getest, afhankelijk van het ras en de vereniging. Het is raadzaam om ouders of voorouders van dieren die nog gebruikt worden in de fok ook op te volgen. Het is veel waard om te weten dat een fokpoes of dekkater ouders of voorouders heeft die op bijvoorbeeld 10 jaar leeftijd nog negatief getest zijn. Hetzelfde geldt voor nakomelingen. Vraag steeds aan diegene waar u een kitten aan verkoopt u op de hoogte te houden, zeker bij plotse sterfte.
Hoe verloopt een echocardiografische screening?
We beginnen met een goede auscultatie waarbij we luisteren naar de hartfrequentie, de regelmaat van de hartslag en of er een hartruis of gallopritme aanwezig is.
Daarna wordt de kat rustig op de rechter zijde gelegd op een speciale echocardiotafel. De eigenaar houdt meestal de voorpoten vast en is op die manier dicht bij het hoofdje om hem/haar gerust te stellen. Als de kat rustig ligt wordt een ECG aangesloten. Ter hoogte van de oksel wordt een klein plukje haar weggeschoren op de plaats waar we echogel aanbrengen en het hart in beeld gaan brengen. Daarna wordt de kat vaak ook op de linker zijde gelegd om nog bijkomende metingen uit te voeren.
Tijdens het onderzoek worden een aantal standaard beelden en filmfragmenten genomen om daarna metingen op uit te voeren. Het echografisch onderzoek zelf duurt zo’n 10 minuten, maar het nauwkeurig uitvoeren van de metingen en het administratieve werk achteraf duurt ongeveer het dubbele.
Bijna alle katten laten dit toe in wakkere toestand. Sedatie (= lichte verdoving of roesje) is dus bijna nooit nodig.
Erfelijkheid en waarom screenen?
HCM heeft een erfelijke basis, maar de overerfbaarheid is erg complex. Er zijn immers veel genmutaties op verschíllende genen, die verantwoordelijk kunnen zijn. HCM is geen aangeboren ziekte. Katten worden met een gezond hart geboren, maar kunnen wel een aantal genen of beter gezegd genmutaties (kleine afwijkingen in de DNA-code) dragen die HCM kunnen veroorzaken op latere leeftijd. Uit verschillende onderzoeken is gebleken dat veel van deze genen niet volledig ‘penetrant’ zijn. Dat wil zeggen, ze zitten er wel, maar ze zijn niet of nóg niet actief. De katten zijn dan ‘drager’ van deze genmutaties terwijl ze toch de ziekte niet of nóg niet hebben (genotype aanwezig, fenotype afwezig).
Waarom genmutaties dan toch plots actief worden (“genexpressie”), is afhankelijk van omgevingsfactoren en misschien ook van andere genen (dus de combinatie van genen of genmutaties). Het is dus best mogelijk dat een kat in zijn jonge jaren negatief test, maar dat de foute genen pas op latere leeftijd actief worden waardoor de kat echografisch dan wel positief test. Een éénmalige echografische test op 1 jaar is dus niet afdoende.
Door de hoeveelheid van genen en genmutaties en de complexe invloed op elkaar is een genetische test als screening methode niet betrouwbaar. Echografische screening van het hart is voorlopig de enige methode om het voorkomen van HCM in de kattenpopulatie te verminderen. Net als bij heupdysplasie bij de hond, sporen we hiermee alleen de katten op die fenotypisch positief zijn (= aanwijzingen op echo die kunnen wijzen op HCM) en dus niet de dragers (fenotype afwezig, genotype aanwezig). Hierdoor is het dus mogelijk dat 2 ouders die op een bepaald moment nog negatief testen toch een kitten voortbrengen dat de ziekte ontwikkelt. Ook kunnen ouders die in het heden nog negatief testen, in de toekomst toch positief worden. Dit maakt echografische screening niet zaligmakend en soms erg frustrerend voor fokkers. Toch moeten we fokkers blijven motiveren om hun fokdieren regelmatig echografisch te screenen zodat de genmutaties zich zo weinig mogelijk verspreiden en het niet catastrofaal wordt. Daarnaast is het raadzaam de ‘lijnen’ in het oog te houden en heel open te communiceren via allerlei kanalen wanneer er een fokdier of nakomeling HCM blijkt te hebben. Deze openheid maakt het gemakkelijker voor fokkers uit te pluizen langs welke kant er iets fout is wanneer men de pech heeft met HCM geconfronteerd te worden. Zo kan nagegaan worden met welke lijnen beter niet verder gefokt wordt.
Toch nog DNA testen?
Zowel voor de Maine Coon als voor de Ragdoll zijn er gentesten beschikbaar die de aanwezigheid van één bepaalde genmutatie (kleine afwijking in het DNA) kunnen opsporen. De mutatie is wel verschillend in beide rassen: A31P bij de Maine Coon en R820W bij de Ragdoll, en de testen zijn niet van toepassing voor andere rassen. Helaas blijkt uit onderzoek dat deze test zelfs bij deze 2 rassen niet betrouwbaar is: er komen evenveel HCM positieve gevallen voor bij Ragdolls of Maine Coons die positief testen op de genmutatie, als bij katten die de genmutatie niet dragen. Dat komt omdat er slechts op één mutatie getest wordt, terwijl er waarschijnlijk nog vele andere mutaties zijn waarvoor we nog niet kunnen testen. Een genetische test is dus voorlopig niet zo zinvol.
Wat zijn de normale referentie intervallen voor linker ventriculaire wand dikte?
Op dit moment is echocardiografie voorlopig de meest waardevolle screeningtest voor HCM. Echter, echocardiografische screening is moeilijk en uitdagend. Het verschil tussen de wanddikte van een normale en HCM-positieve kat is soms slechts een fractie van een millimeter. Gelukkig is de laatste jaren door vooruitgang in de technologie, de beeldkwaliteit en resolutie enorm verbetert. Echter de specialist die het onderzoek uitvoert moet uiterst getraind zijn en over een consistente techniek beschikken om de juiste metingen uit te voeren. En zelfs dan blijft het voor ervaren specialisten soms nog moeilijk in sómmige gevallen. HCM heeft verschillende verschijningsvormen. Het kan zijn dat alleen het septum of alleen de vrije wand, of een deel van het septum of vrije wand, of zelfs alleen de apex of de papillair spieren verdikt zijn. Soms is er ook een gegeneraliseerde verdikking van de hele wand.
Omdat er zoveel verschillende verschijningsvormen zijn moet men beelden in M-mode (Fig 4 B, C, D) combineren met metingen in 2-D (Fig 4 A). M-mode beelden worden standaard genomen net onder de mitralis klep. Ze kunnen lokale verdikkingen missen, of omgekeerd de wanddikte overschatten doordat een deel van de papillair spier mee wordt gemeten indien de cursor niet correct wordt geplaatst.
De bovengrens voor een normale wanddikte in eind-diastole (= einde van de ontspanningsfase) was vroeger 5.5 mm, maar recente studies tonen aan de bovengrens lager ligt (rond de 5 mm).
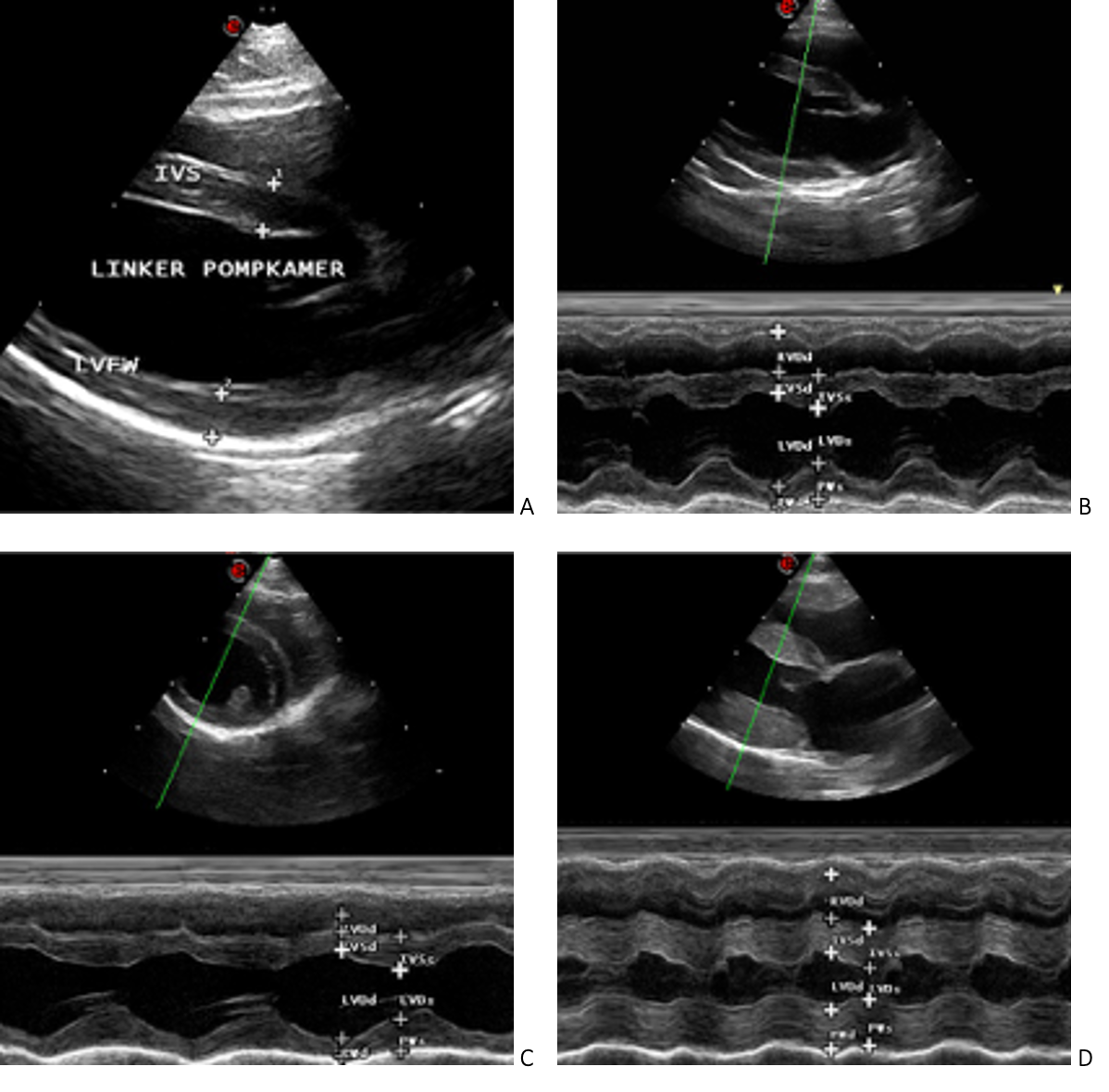
A. Normaal hart met 2-D metingen van interventriculair septum en linker ventrikel vrije wand. B. M-mode metingen long-axis (LAX). C. M-mode metingen short axis (SAX). D. M-mode LAX van HCM positief
Hoewel in de meeste studies gewicht geen parameter was, hebben grote katten, zoals erg grote Maine Coons waarschijnlijk een iets hogere linker ventrikel wanddikte, die tot en zelfs voorbij 5 mm kan reiken zonder een indicatie voor HCM. Een recente studie bij Bengalen toonde aan dat ook bij dit ras de dikte van het interventriculair septum hoger was vergeleken met de gemiddelde waarden van de globale kattenpopulatie. Er waren ook verschillen in dikte afhankelijk van lichaamsgewicht, en onafhankelijk van het lichaamsgewicht ook verschillen tussen beide geslachten, waarbij katers gemiddeld een iets dikkere wand hadden dan poezen.
Omdat er een overlap is tussen een normaal hart en milde HCM, is er veel controversie betreffende katten die een wanddikte hebben net aan de bovengrens en er iets boven (tussen 5 en 6 mm). Daarom is het soms onmogelijk om met zekerheid het onderscheid tussen HCM-positief en normaal te kunnen maken. Sommige screening programma’s zoals PawPeds laten toe katten als “equivocal” te beoordelen, wat wil zeggen dan men niet met zekerheid kan zeggen of de kat al dan niet normaal of HCM positief is. Bij deze katten kan regelmatige echografische hercontrole helpen om HCM uit te sluiten of te bevestigen.
Scherp afgelijnde endocardiale randen zijn nodig voor exacte metingen. In M-Mode is ‘leading-edge-to leading-edge’ techniek (Fig 5 B) standaard en deze techniek wordt door de meeste specialisten ook toegepast.
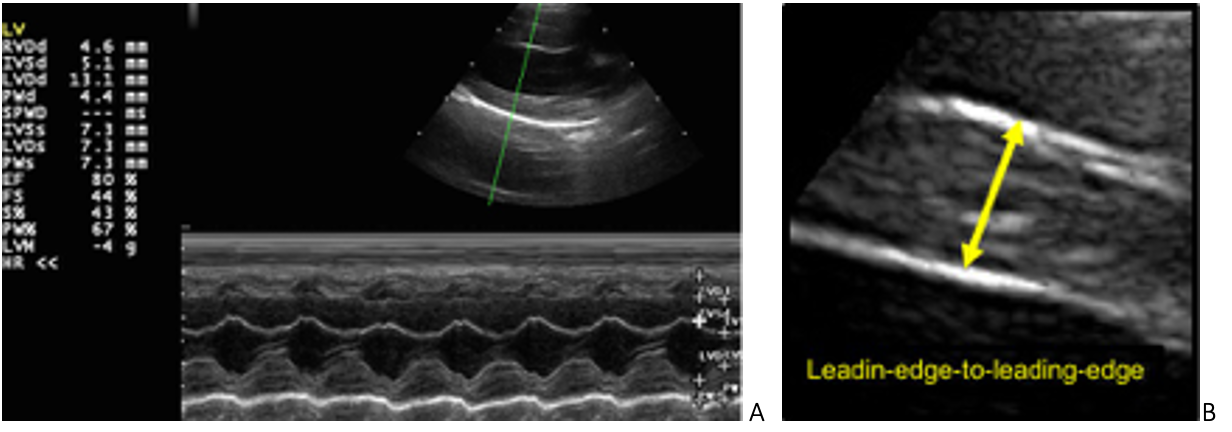
A M-mode meting van een jonge Britse Korthaar. Het IVSd (septum in diastole=ontspanningsfase) is net over de 5 mm. Dit is eigenlijk net aan de bovengrens maar verder waren er geen afwijkingen (geen hartruis, geen SAM, E/A normaal). Het is bijzonder moeilijk om in dit geval te weten of ze werkelijk positief is, of het een kat is die weliswaar een dikke wand heeft, maar mogelijks nooit HCM zal ontwikkelen. B. Detailbeeld van leading-edge-to-leading-edge: dit wil zeggen dat men van de bovenrand van de endocardiale rand tot de bovenrand van de volgende endocardiale rand meet.
Wat zijn ”false tendons” of “moderator bands”?
False tendons zijn een soort koordjes die de ventrikels doorkruisen. Ze verlopen meestal van een papillair spier naar het septum of de ventrikel vrije wand. De klinische betekenis van deze false tendons is niet gekend. Het kan een normale bevinding zijn, maar soms veroorzaken ze een focale verdikking van het septum of hechten ze vast op ectopisch papillair spierweefsel. Hierdoor is het soms erg moeilijk om het interventriculair septum correct te meten, zelfs door ervaren specialisten, en het verkeerdelijk als HCM te beschouwen. Het is belangrijk te werken met een high-end toestel met hoge resolutie en frame-rate. Alsook is het belangrijk om het septum op verschillende manieren te meten, zowel in 2-D als op M-mode en indien nodig moet men met sine loop beeld per beeld analyseren.
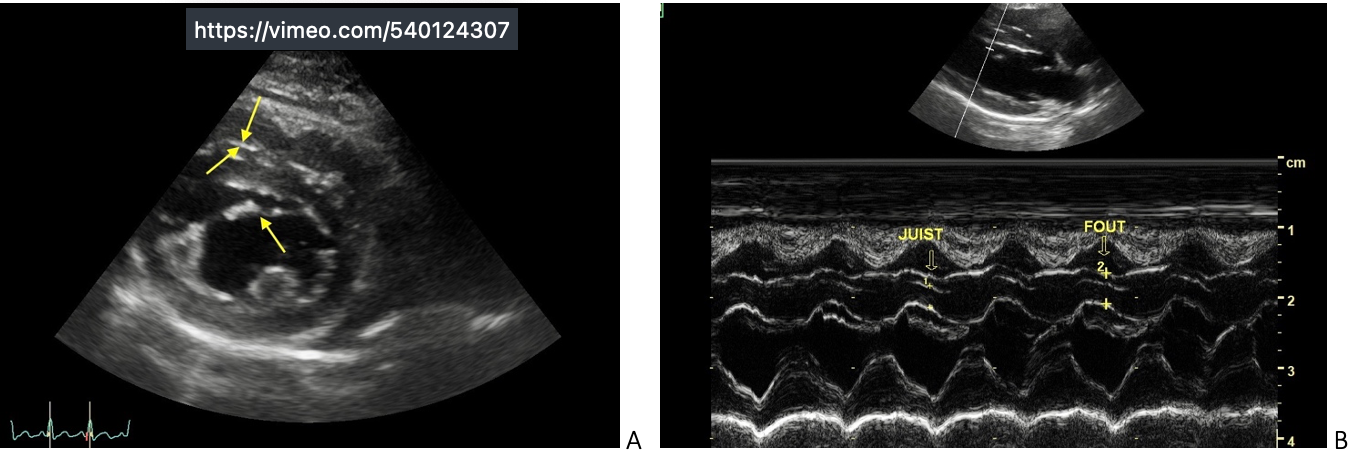
A. SAX-beeld van een hart met moderator bands (gele pijlen). Er loopt één in het linker ventrikel van de anterieure papillair spier naar het septum en één in het rechter ventrikel evenwijdig met het septum. B. M-mode beeld van hetzelfde hart. Indien je de moderator band fout mee incalculeert bij de meting van het septum dan kom je een hogere waarde uit dan het septum werkelijk is, waardoor een kat soms foutief als HCM positief wordt bestempeld. Hier is het nu duidelijk, maar soms is het onderscheid tussen werklijke endocardiale wand of moderator band, zeker op M-mode, erg moeilijk.
Wat zijn papillair spieren?
De papillair spieren zijn uitstulpingen in de wand van het hart die door middel van kleine peesjes verbonden zijn met de hartkleppen, die zich tussen boezems en kamers bevinden. Ze verhinderen dat de hartkleppen doorslaan. Hypertrofie (vergroting) van de papillair spieren is iets wat we zien bij HCM en bij sommige katten kan dit zelfs het eerste teken zijn van HCM. De morfologie van de papillair spieren wordt meestal subjectief beoordeeld, maar er zijn ook methodes beschreven om ze te meten. Het is erg moeilijk om de papillair spieren te beoordelen gezien er zoveel verschil is in vorm tussen katten. Bovendien is er geen consensus over hoe variaties in morfologie van papillair spieren moeten geïnterpreteerd worden in de context van HCM screening.
Videofragment van linker pompkamer in dwarsdoorsnede van een hart met vergrote papillair spieren.
Wat is SAM (Systolic Anterior Motion van de Mitralis klep)?
SAM houdt in dat de voorste mitralisklep naar het septum toe beweegt tijdens de contractie-fase (systole) waardoor er tijdelijk een vernauwing van de linker ventrikel outflow tract ontstaat waardoor klep insufficiëntie en turbulentie van bloed optreedt. Dit veroorzaakt in de meeste gevallen een hartruis. Soms treedt SAM alleen op bij excitatie of als het hartritme toeneemt, en is het afwezig als de kat rustig of verdoofd is. Sommige katten vertonen SAM zonder linker ventrikel hypertrofie en anderzijds vertonen niet alle HCM positieve katten SAM. Er is controversie of SAM een normale bevinding kan zijn of dat het een indicator is van HCM, zelfs al is de linker ventrikel wand niet verdikt.
Videofragment van HCM positieve kat met SAM.
SAM veroorzaakt een tijdelijke insufficiëntie van de mitraliskleppen. Op colour doppler ziet men dan een typische gelijktijdige aliasing in de ingang van aorta en een kleine regurgitatie-jet ter hoogte van de mitralis kleppen.
Zijn er nog andere oorzaken van HCM?
Ja die zijn er, maar de meeste komen bijna alleen voor bij oudere katten (>8 j): hyperthyroïdie (te hard werkende schildklier), acromegalie (zeldzame aandoening die we soms bij diabetes katten zien), chronisch nierfalen en hypertensie (hoge bloeddruk). Naast deze ouderdomsziekten kan ook aortastenose (vernauwing van de hoofdslagader) verdikking van de hartspier geven. Aortastenose is een aangeboren hartafwijking en is bij katten uiterst zeldzaam.
Myocarditis of een hartspierontsteking kan ook aanleiding geven tot verdikking van de hartspier. Myocarditis kan veroorzaakt worden door een bacterie, virus, schimmel of ééncellig organisme, maar kan ook immuun-gemedieerd zijn. Een hartspier verdikking door primaire HCM kan echografisch niet van myocarditis onderscheiden worden. Katten met myocarditis hebben meestal een voorgeschiedenis van een andere ziekte zoals een longontsteking, abces, virale infectie…
Men spreekt in de literatuur ook soms over ‘pseudohypertrofie’. Dat kan gebeuren wanneer de kat erg uitgedroogd is en het bloedvolume aldus lager is. Dit heeft tot gevolg dat de spierwand minder uitrekt tijdens de vullingsfase en daardoor de wand net iets dikker lijkt. Meestal zijn fokdieren gezond en is die kans daarop klein. Omgekeerd kan lactatie of dracht het bloedvolume erg doen toenemen, wat een meer uitgerekte toestand van de hartspier als gevolg heeft en dus aanleiding kan geven tot lagere waarden. Daar moet men rekening mee houden wanneer men drachtige of lacterende dieren screent.
Meer over het ziekte verloop van HCM.
Referenties:
- Meurs KM, Sanchez X, David RM, Bowles NE, Towbin JA, Reiser PJ, Kittleson JA, Munro MJ, Dryburgh K, Macdonald KA, Kittleson MD. A cardiac myosin binding protein C mutation in the Maine Coon cat with familial hypertrophic cardiomyopathy. Hum Mol Genet 2005;14: 3587e3593.
- Meurs KM, Norgard MM, Ederer MM, Hendrix KP, Kittleson MD. A substitution mutation in the myosin binding protein C gene in Ragdoll hypertrophic cardiomyopathy. Genomics 2007;90:261e264.
- Fries R, Heaney AM, Meurs KM. Prevalence of the myosinbinding protein C mutation in Maine Coon cats. J Vet Intern Med 2008;22:893-896.
- Wess G, Schinner C, Weber K, Kuchenhoff H, Hartmann K. Association of A31P and A74T polymorphisms in the myosin binding protein C3 gene and hypertrophic cardiomyopathy in Maine Coon and other breed cats. J Vet Intern Med 2010; 24:527-532.
- Borgeat K, Casamian-Sorrosal D, Helps C, Luis Fuentes V, Connolly DJ. Association of the myosin binding protein C3 mutation (MYBPC3 R820W) with cardiac death in a survey of 236 Ragdoll cats. J Vet Cardiol 2014;16:73-80.
- Longeri M, Ferrari P, Knafelz P, Mezzelani A, Marabotti A, Milanesi L, Pertica G, Polli M, Brambilla PG, Kittleson M, Lyons LA, Porciello F. Myosin-binding protein C DNA variants in domestic cats (A31P, A74T, R820W) and their association with hypertrophic cardiomyopathy. J Vet Intern Med 2013;27:275-285.
- Häggström J, Luis Fuentes V, Wess G. Screening for hypertrophic cardiomyopathy in cats. J Vet Cardiol 2015;17, 134-149.
- Peterson EN, Moise NS, Brown CA, Erb HN, Slater MR. Heterogeneity of hypertrophy in feline hypertrophic heart disease. J Vet Intern Med 1993;7:183-189.
- Bonagura JD. Feline echocardiography. J Feline Med Surg 2000;2:147-151.
- Wagner T, Fuentes V, Payne J, McDermott N, Brodbelt D.Comparison of auscultatory and echocardiographic findings in healthy adult cats. J Vet Cardiol 2010;12:171-182.
- Gundler S, Tidholm A, Ha¨ggstro¨m J. Prevalence of myocardial hypertrophy in a population of asymptomatic Swedish Maine Coon cats. Acta Vet Scand 2008;50:22.
- Ha¨ggstro¨m J, Falk T, Nilsfors L, Olsson U, Dajm A, Kresken JG, Ljungvall I, Ho¨glund K, Tidholm A. M-mode measurement of left ventricular wall thickness in a large population of screened cats with or without hypertrophic cardiomyopathy. Proc. 2011 ACVIM Forum, Denver, USA, June 14-18, 2011 (research report).
- Drourr L, Lefbom BK, Rosenthal SL, Tyrrell Jr WD. Measurement of M-mode echocardiographic parameters in healthy adult Maine Coon cats. J Am Vet Med Assoc 2005; 226:734-737.
- Freeman LM, Rush JE, Meurs KM, Bulmer BJ, Cunningham SM. Body size and metabolic differences in Maine Coon cats with and without hypertrophic cardiomyopathy. J Feline Med Surg 2013;15:74-80.
- Dirven MJ, Cornelissen JM, Barendse MA, van Mook MC, Sterenborg JA. Cause of heart murmurs in 57 apparently healthy cats. Tijdschr Diergeneeskd 2010;135:840-847.
- Adin DB, Diley-Poston L. Papillary muscle measurements in cats with normal echocardiograms and cats with concentric left ventricular hypertrophy. J Vet Intern Med 2007;21: 737-741.
- Wolf OA, Imgrund M, Wess G. Echocardiographic assessment of feline false tendons and their relationship with focal thickening of the left ventricle. J Vet Cardiol 2015
- Brian A Scansen, Kyla L Morgan. Reference intervals and allometric scaling of echocardiographic measurements in bengal cats. J Vet Cardiol 2015;17:282-295.